《有机硅材料》2011年第25卷第1期
硅溶胶中钠离子含量的准确测定
翟丽莉,王 珍,鲍 慧,季晓玲*
(大连斯诺化学新材料科学技术有限公司,辽宁大连116015 )
摘要:采用火焰光度计法测定普通碱性钠型硅溶胶中钠离子含量,研究了前处理方法对测定结果的影响,并用已知钠离子浓度的硅溶胶对该方法进行验证。结果表明,较佳前处理方法是 SiO2、氢氟酸和消解液按1:6:0.5的量之比混合,常温反应15 min;再稀释200~600倍,然后采用火焰光度计进行测定;验证实验结果表明,该法准确度和精密度均较好。
关键词:硅溶胶,钠离子,火焰光度计,二氧化硅,氢氟酸,Na2O
中图分类号:TQ127.2 文献标识码:A 文章编号:1009-4369(2011)01- 0036-04
硅溶胶是无定形二氧化硅粒子的水分散液,其分子通式可表示为mSiO2·nH2O。不同类型、不同性质的硅溶胶的应用领域不同。影响硅溶胶性质的因素很多,钠离子含量是其中之一。若钠离子含量太高,则硅溶胶的耐水性、物理强度、成膜性都会变差,从而影响它在铸造、催化剂等领域的应用[1]。如用于彩色显像管时,若钠离子和钾离子含量过高会严重影响显像管的色彩和使用寿命[2]。所以硅溶胶中钠离子含量的准确测定很重要。
目前测定钠离子的方法主要有:钠离子浓度计法、离子色谱法、火焰光度计法[3-4]。其中第一种方法的实验仪器准确度较差,测得结果相对标准偏差较大;若硅溶胶为铵型,则测试结果无意义。后两种方法需配制系列标准溶液,实验过程较复杂且离子色谱仪器昂贵。准确测定硅溶胶中钠离子含量的关键是硅溶胶样品的前处理,若处理不当,则不能将钠离子从胶粒中全部释放,导致测量数据重复性不好,且结果偏低。为此本实验对普通碱性钠型硅溶胶样品的处理方法进行了探讨。且用自制的已知钠离子浓度的硅溶胶对该法进行了验证。
1 实验
1.1 主要试剂及仪器
硅粉:纯度99.99%,沛县天纳源硅材料有限公司;氢氧化钠:AR,沈阳化学试剂厂;氢氟酸(HF):AR,沈阳化学试剂厂;氯化钠:基准试剂,上海化科实验器材有限公司;消解液:主要成分硝酸,自制。
分析天平:感量0.0001g,AL204型,梅特勒-托利多仪器公司;马福炉:SX-2.5-10型,上海圣欣科学仪器有限公司;火焰光度计:FP640型,发射型,上海傲谱分析仪器有限公司;旋转黏度计:NDJ-1,上海天平仪器厂;精密pH计:PHS-3C型,上海雷磁仪器厂;比重计:KEM型,上海图新电子科技有限公司。
1.2 实验过程
1.2.1 钠标准溶液的配制
准确称取经550℃恒重的氯化钠0.585 0 g,溶于去离子水中,定容至1 L,得浓度为0.01 mol/L的钠离子标准溶液,记为PNa2溶液;再将PNa2标准溶液分别稀释10倍和100倍,得到PNa3、PNa4钠离子标准溶液。
1.2.2硅溶胶样品的处理
用聚乙烯瓶准确称取一定量硅溶胶,按SiO2、氢氟酸、消解液的量之比〔n(SiO2):n(HF):n(消解液)〕为1:6:0.5依次加入氢氟酸和消解液,常温反应15 min;用去离水稀释至一定倍数。
1.2.3钠离子含量的测定过程
硅溶胶中的钠离子含量常以Na2O的质量分数[w(Na2O)]计。待火焰光度计预热稳定后,分别用PNa3、PNa4钠离子标准溶液调满标(窗口显示100)和调低标(窗口显示0),重复调试直至满标和低标显示值稳定。测定按1.2.2节处理的稀释液,记录显示值,按式1计算w(Na2O)。
w(Na2O)=[显示值/100×(10-3—10-4)+10-4]×N×M/2ρ ×100% (1)
式中, N为样品的稀释倍数;ρ为硅溶胶的密度,g/cm3;M为氧化钠的相对分子质量。
1.2.4 已知钠离子含量的硅溶胶制备
将硅粉、水和氢氧化钠按一定质量比放入反应器中,搅拌反应约5 h,直至无反应残渣,得硅溶胶A~D号样品;称量并测其SiO2含量[5]。按式2计算w(Na2O)。
w(Na2O)=mNaOH×62/(2×4×mSi-sol) ×100% (2)
式中,mNaOH为反应时加入氢氧化钠的质量,g;mSi-sol为反应后所得的硅溶胶总质量(因反应后容器内无固体的硅粉,所以硅粉转换率视为100%),g;去离子水的质量均为850 g。
2 结果与讨论
2.1 硅溶胶样品处理条件的筛选
钠离子作为胶体稳定剂被吸附在二氧化硅胶粒的表面,形成Si—O—Na结构,也有部分钠离子在胶粒的生成过程中被夹杂进胶粒内部;所以,若样品处理不好,将导致钠离子不能完全游离,使测定结果偏低。二氧化硅胶粒与氢氟酸在水相的反应方程式为:
SiO2+6HF=H2SiF6+2H2O
氟硅酸是络合卤酸,中心离子Si4+与弱酸根F-形成了较强的配位键,迫使H+移到络离子的外界,变得容易电离,酸性增强,体系易生成氟硅酸钠。氟硅酸盐中以钠盐的溶解度最低,25 ℃时氟硅酸钠在水中的溶解度只有0.78%;为使待测钠离子完全游离,体系中需另外加入消解液。消解液的加入量对w(Na2O)的影响见图1,处理条件为n(SiO2):n(HF)=1:6,常温反应15 min。
由图1可见,消解液的加入量达到n(消解液) :n(SiO2) 达到0.5后,w(Na2O)值变化很小。
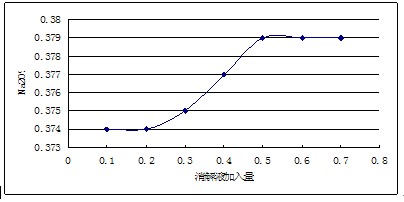
图1 消解液加入量对w(Na2O)测定结果的影响
表1是5种处理条件对硅溶胶B样品w(Na2O)值的影响。由表1可见,测定结果的相对标准偏差都小于1%,平均值0.379%与B样品的理论w(Na2O)值0.380%的相对误差为0.105%;即1#~5#处理条件均可。
表1处理条件对硅溶胶B的w(Na2O)测定结果的影响
|
编号 |
n(SiO2):n(HF):n(消解液) |
处理条件 |
w(Na2O)/% |
RSD(n=6)/% |
|
1# |
1:6:0.5 |
常温×15 min |
0.379 |
0.67 |
|
2# |
1:6:0.5 |
60℃×60 min |
0.379 |
0.65 |
|
3# |
1:6:0.5 |
80℃×60 min |
0.380 |
0.63 |
|
4# |
1:6.1:0.5 |
常温×15 min |
0.379 |
0.62 |
|
5# |
1:6.2:0.5 |
常温×15 min |
3.80 |
0.60 |
综上所述,样品的前处理条件选择n(SiO2):n(HF):n(消解液)=1:6:0.5、常温反应15 min。
2.2 稀释倍数对w(Na2O)值测定结果的影响
稀释倍数会影响硅溶胶的电离程度,以前的方法对稀释倍数很敏感,对测试结果影响很大。
FP640型火焰光度计在钠离子浓度为10-3~10-4 mol/L的范围内线性很好。将硅溶胶B按1#条件处理后,用去离子水稀释200、300、400、500、600倍,测定w(Na2O)值,结果见表2。倘若钠离子没有全部释放,不同的稀释倍数对测定值会有明显影响。由表2可见,稀释倍数对w(Na2O)值测定结果无明显影响,但显示值必须落在0~100的量程范围内。因此,在实验室或生产中只需测一个稀释倍数的样品即可,为快速测定创造了条件。该实验同时也证明,1.2.2的前处理方法是可行的。
表2 稀释倍数对w(Na2O)测定结果的影响
|
实际稀释倍数 |
实测显示值 |
w(Na2O)/% |
|
实测值 |
算术均值(n=6) |
RSD(n=6) |
|
200.30 |
70 |
0.379 |
0.379 |
0.71 |
|
300.25 |
43 |
0.379 |
0.380 |
0.59 |
|
396.23 |
30 |
0.380 |
0.379 |
0.63 |
|
507.29 |
21 |
0.380 |
0.380 |
0.68 |
|
599.26 |
16 |
0.379 |
0.379 |
0.65 |
2.3 w(Na2O)值测定方法验证
对已知w(Na2O)值的硅溶胶A~D号样品(基本参数列于表3)按1#方法处理,稀释300倍后测定w(Na2O)值,结果见表3。
由表3可见,w(Na2O)的测定值相对误差及相对标准偏差都很小,从而证明1#处理方法及测试方法都是可行的。
表3 已知w(Na2O)值的硅溶胶的验证实验结果
|
测试项目 |
硅溶胶 |
|
|
A |
B |
C |
D |
|
m(Si) /g +m(NaOH) /g |
140+4.52 |
140+4.82 |
140+5.29 |
140+5.82 |
|
密度/g·cm-3 |
1.198 |
1.196 |
1.202 |
1.192 |
|
pH值 |
9.31 |
9.87 |
10.23 |
10.52 |
|
硅溶胶的质量浓度/% |
29.80 |
29.50 |
30.11 |
30.02 |
|
硅溶胶总量/g |
1006.70 |
1016.90 |
996.35 |
999.33 |
|
w(Na2O)/% |
|
|
|
|
|
理论 |
0.350 |
0.380 |
0.410 |
0.451 |
|
实测 |
0.349 |
0.378 |
0.408 |
0.449 |
|
算术均值(n=6) |
0.349 |
0.379 |
0.409 |
0.449 |
|
相对误差(n=6) |
0.286 |
0.263 |
0.268 |
0.263 |
|
RSD(n=6) |
0.62 |
0.68 |
0.59 |
0.65 |
3 结论
普通碱性钠型硅溶胶样品的较佳前处理方法是 将SiO2、氢氟酸和消解液按1:6:0.5的量之比混合,常温反应15 min;再稀释200~600倍,然后采用火焰光度计进行测定。采用此法测得的Na2O质量分数的准确度和精密度均较好。该法也适用于其它类型硅溶胶中Na2O质量分数的测试,但需预先粗测确定合适的稀释倍数以保证显示值落在0~100的量程内,超过100或显示负数说明稀释倍数不够或稀释倍数过大,都需要调整到0~100间较好的线性范围内。该法也适用于硅溶胶中钾离子、钙离子和镁离子含量的测定。该法快速、经济,无需配制系列标准溶液和昂贵仪器,非常适合硅溶胶生产企业的在线监测和用户对钠离子含量的检测。
参考文献
[1] 王宇湖,张宁.耐碱性超高纯硅溶胶的制备方法: CN101012060A[1] [P].2007-08-08.
[2] 潘国顺,顾忠华,路新春等.一种超高纯二氧化硅溶胶的纯化方法: CN101475180A [P].2009-07-08.
[3] 王少明,赵华. 离子色谱法测定高纯硅溶胶标准物质中的钠、钾、钙、镁[J]. 化学分析计量, 2009, 18(3): 42-44.
[4] 黄慧敏. 火焰原子吸收分光光度法测定环境水样中钠和钾[J]. 福建分析测试, 2007, 16(2): 115-116.
[5] 王珍,季晓玲,翟丽莉. 提高单质硅生产硅溶胶硅粉转化率的研究[J]. 有机硅材料, 2010, 24(2): 95-97.
Accurately measured contents of sodium ions in silica sol
ZHAI Li-li, WANG Zhen, BAO Hui , JI Xiao-ling*
(SNOWCHEMICAL S &T CO.LTD , Liaoning Dalian 116015 , China )
Abstract: The colloid particles silica sol was reacted with hydrofluoric acid and digestion solution .So the sodium ions which was used for stabilizing colloid particles was set free. The above reaction liquid was diluted with deionized water to some multiple then using emission type flame photometer measured contents of sodium ions. Besides we carried on the proof test that we detected contents of sodium ions in self-prepared silicon sol which contents of sodium ions was known. The results showed that the accuracy and precision of this method was better. This method needn't prepare series of standard solutions and costly instruments. The merits of method were accurate, fast and economical. This method was specially fit for companies detected sodium ions during process of produced silicon sol and users.
Keywords: silicon sol, sodium ion, emission type flame photometer,silicon dioxide ,hydrofluoric acid ,Na2O
|


