注:如需PDF原文,请将E-mail发送至本公司邮箱,注明所需文章即可。
陈永熙 周立娟,李英霞 雷家珩
摘 要:采用Y2O3 为原料先制得无水YCl3 然后与异丙醇反应生成YCl3·3C3H7OH 加合物,并采用自制异丙醇钠与之反应制备得到异丙醇钇,反应的最佳条件为80 ℃回流3~4 小时,然后静置12h 以便NaCl 的分离。在YCl3·6H2O 脱水制备YCl3 的过程中,采用醋酸酐脱水法,具有方法简单,污染小,且易于操作等特点。
关键词:异丙醇钇的制备;金属醇盐的合成;乙酸酐脱水法;陶瓷复合材料
1 前言
随着高技术陶瓷的发展,陶瓷晶界工程和纳米技术已成为获取高性能材料的主要手段。高技术陶瓷很多重要的性质取决于晶界。20 世纪50年代发展起来的金属醇盐化学为高技术陶瓷晶界工程的精细化和“原子”层次上的掺杂提供了重要依据。
金属醇盐又称为金属酸酯或金属烷氧基化合物,是被人们誉为填补了有机化学和无机化学之间空白的广义金属化合物的一部分,它们的分子结构中至少有一个M-O-C 单元(M 代表金属离子)。因为氧原子呈较强的电负性,故金属醇盐常显示出一定的极性。但大多数金属醇盐在有机溶剂中表现出的相当程度的溶解性,又使它们具有共价化合物的一些特征。因此,金属醇盐是一类很好的可用于无机复合材料前驱物分散和掺杂的重要的添加剂。
本工作以氧化钇为原料,通过自制的无水三氯化钇制备三氯化钇-异丙醇加合物,然后再与异丙醇钠反应,成功地合成了异丙醇钇。它在碳化硅晶须增韧陶瓷复合材料、PTC 钛酸钡陶瓷、氧化钇纳米粉体的制备等方面具有广泛的用途。
2 实验
本工作制备异丙醇钇所采用的合成路线为:
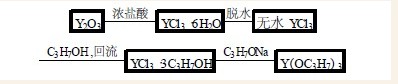
2. 1 主要的试剂与仪器设备
异丙醇(A. R. ):按100g/ L 的量加入氧化钙,静置24h ,回流3~4h,收集82~83 ℃馏分,以除去其中少量水分,储于干燥器中备用;
苯(A. R. ):按100g/ L 的量加入无水氯化钙,静置24h,回流3~4h,收集80 ℃馏分,储于干燥器中备用;
金属钠(A. R. ):保存于煤油中,使用时用滤纸迅速吸干煤油,按所需量迅速切取;
氧化钇(A. R. ):Y2O3 含量≥99. 9 %;
浓盐酸(A. R. ):密度为1. 18~1. 19g·cm-3 ;
乙酸酐(A. R. ):密度为11080g·cm-3 。
用于脱水及合成用的玻璃仪器均为标准磨口玻璃仪器,而且使用前均需洗净烘干,使用时用真空脂密封。
2. 2 无水氯化钇的制备
由于异丙醇钇是一种极易水解的醇盐,因此,合成时仪器的干燥以及原料的脱水是异丙醇钇合成的 关键。通常氯化钇晶体中含有6~7 个结晶水,通过一般的加热方法难以除去。我们采取以下2 种方法对氯化钇脱水进行研究:
(1)大量NH4Cl 作用下的加热脱水法
把Y2O3 及NH4Cl 按1∶4(质量比)的比例称取,并加入适量浓HCl,于蒸发皿中低温蒸干,再加入同量的浓HCl,再次蒸干。把所得产物置于硬质玻璃管中,通入干燥的氯气,并加热,直至NH4Cl 全部升华为止。
(2) 乙酸酐脱水法
按1g Y2O3加入10mL 浓HCl 的比例加入Y2O3及浓HCl 在调温电炉上低温蒸发至干,将所得的产物研细后加入50mL 乙酸酐,用磁力搅拌器搅拌4h,再静置2 天后用抽滤瓶抽滤,用已脱水的苯洗涤2~3 次,便得到白色无水YCl3 粉末。
2. 3 三氯化钇-异丙醇加合物的制备
将上述用乙酸酐脱水所得的无水YCl3 在隔绝空气的条件下用红外灯处理,以除去其中残留的苯及乙酸酐等物质。再加入80mL 异丙醇,在500mL 圆底烧瓶中低温回流2h。
2. 4 异丙醇钠的制备
称取一定量的金属钠,加入到80mL 苯和40mL 异丙醇的混合液中,使金属钠与异丙醇完全反应,生成的异丙醇钠溶解于苯和异丙醇的混合液中。
2. 5 异丙醇钇的合成
将所得的加合物YCl3·3C3H7OH 和异丙醇钠溶液同时转移到烧瓶中,充分振荡,此时由于反应放热须在80 ℃下回流3~4h,静置12h,使生成的氯化钠晶体与异丙醇钇的溶液分层,然后抽滤,用异丙醇洗涤2 次,将滤液减压蒸馏便得到白色泡沫状的异丙醇钇固体。
2. 6 测试与分析
2. 6. 1 无水三氯化钇的鉴定
称取一定量上述脱水的YCl3,将其溶于稀盐酸中,调节pH = 5~6,以二甲酚橙作指示剂,用EDTA 进行络合滴定,测得YCl3 中Y的质量分数为45.48 %,而YCl3 中Y 的理论质量分数为45.52 %,相对误差小于0. 1 %,说明乙酸酐脱水法制得的无水YCl3 质量很好。
2. 6. 2 异丙醇钇的红外光谱分析
我们用美国尼高力公司生产的傅立叶变换红外光谱仪对异丙醇钇进行了定性分析(见图1)。
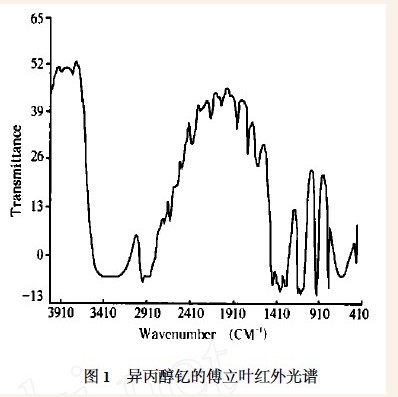
结果表明,样品中异丙氧基在1168cm-1及1129cm-1的特征吸收峰、异丙氧基与取代同一碳原子的二甲基结构的双重特征吸收峰1364cm-1以及异丙醇钇的特征吸收峰1376cm-1,与文献报道结果完全相符。
2. 6. 3 异丙醇钇的热重分析
异丙醇钇的热重分析曲线(见图2)表明:在加热过程中,醇盐随着温度的升高而发生分解,其分解温度为307 ℃左右(在氩气气氛中)。在此阶段,由于Y(OC3H7)3 受热分解生成了Y2O3 及挥发性的C3H7OH 及CH3-CH = CH2 造成重量损失,对所生成的固态产物用ICP2AES 发射光谱法进行分析,在固态产物中Y2O3 的含量高达99. 94 %,其热分解反应式为:
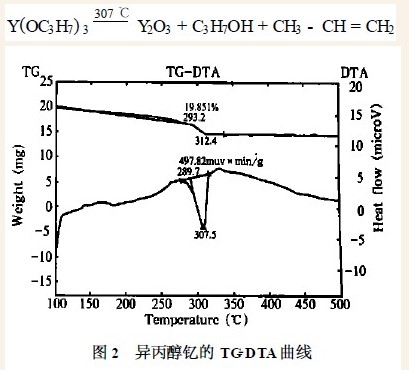
此结果与Mazdiyasni报导的99. 90 %几乎相同。
2. 6. 4 异丙醇钇的元素分析
为了进一步鉴定合成产物,我们采用络合滴定法对Y(OC3H7)3 中钇(Y) 的质量分数进行了滴定。经测定,其中Y的质量分数为33. 35 %,而异丙醇钇Y(OC3H7)3 中Y的质量分数的理论值为33. 43 %,二者十分接近,由此可进一步证实合成的产物为异丙醇钇。
3 结果与讨论
3. 1 氯化铵加热脱水法制备无水氯化钇时产生的尾气含有大量的氯气,需对其进行处理;而乙酸酐脱水法其脱水能力极强,不但使YCl3·6H2O 脱水彻底,而且没有副产物、没有氯气污染,装置简单、脱水效果好,因此通过实验对比本文最后选择了后者作为制备无水氯化钇的脱水方法。
3. 2 根据“相似相溶”原理,由于加合物YCl3·3C3H7OH 在有机溶剂中有较大的溶解度,增加了反应体系中YCl3 的浓度,有利于它与C3H7ONa 的反应。
采用无水YCl3 与C3H7OH 反应,1g 无水YCl3需45mlC3H7OH,体系加热至80 ℃并恒温回流约2h,制得的YCl3·3C3H7OH 加合物产率较高,其反应式为:
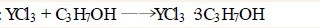
3. 3 YCl3·3C3H7OH 和C3H7ONa 以理论计量比混合,实验证明恒温80 ℃回流3~4h 并静置12h 可使反应进行完全并使生成的NaCl 晶体与Y(OC3H7) 3的溶液较好地分离。其有关反应为:
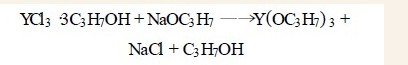
通过实验对比,该途径比用YCl3 与C3H7ONa直接反应合成异丙醇钇的产率高10 %。
4 结论
(1)本文以Y2O3 为起始物,通过合成Y(OC3H7)3的前驱物无水YCl3 、YCl3·3C3H7OH ,最后以YCl3·3C3H7OH 与自制C3H7ONa 反应制得了高纯Y(OC3H7)3。
(2)在无水YCl3 的制备过程中,选用乙酸酐作脱水剂与氯化铵加热脱水法相比,具有脱水效果好、没有氯气的污染,且装置简单等特点。
(3)本工作采用YCl3·3C3H7OH 与C3H7ONa 合成Y(OC3H7)3,增加了YCl3 在有机溶剂中的溶解度,有利于Y(OC3H7)3的生成。其Y(OC3H7)3 的最佳合成条件为80 ℃回流3~4h,然后静置12h,以便于NaCl 的分离。
|


